Effetto Brexit: riparte la sperimentazione italiana dei farmaci

Aifa: salto di qualità per gli studi in ambito pediatrico. La maggioranza dei farmaci ospedalieri utilizzati per i piccoli pazienti non è stata testata su di loro
Farmaci per le malattie del cuore, del respiro, della pelle, degli occhi e, soprattutto, tumori. Tornano a crescere, in Italia, le sperimentazioni cliniche: nel 2018 ne sono state autorizzate 100 in più rispetto al 2017. A tracciare il bilancio è il 18/mo Rapporto nazionale sulla Sperimentazione Clinica dei medicinali dell'Agenzia Italiana del Farmaco (Aifa), da cui emerge "per la prima volta un balzo in avanti" per gli studi in ambito pediatrico: un dato accolto positivamente dai pediatri, visto che la maggioranza dei farmaci ospedalieri utilizzati per i piccoli pazienti non è stata testata su di loro.
Necessari per trovare cure sempre migliori, i nuovi studi clinici autorizzati in Italia nel 2018 sono stati in tutto 666, a fronte dei 565 del 2017. Un numero importante anche perché in contrasto con la costante contrazione delle sperimentazioni a livello europeo: oggi quelle condotte in Italia rappresentano il 20% del totale in Europa. In particolare, i trial messi a punto per studiare farmaci per i minori passano da 51 a 76 e diventano l'11,4% del totale, rispetto al 9% dello scorso anno e degli anni precedenti. "I bimbi non sono dei 'piccoli adulti' e hanno diritto ad avere farmaci sperimentati per loro. In ambito ospedaliero, però, circa il 70% di quelli che gli vengono prescritti è off label, ovvero non registrati per l'età pediatrica", spiega all'Ansa Luisa Galli, referente del gruppo di studio di farmacologia pediatrica della Società Italiana di Pediatria (Sip). Ciò deriva dal fatto che fare studi clinici in ambito pediatrico non è facile, aggiunge, "c'è meno interesse delle aziende e più difficoltà a reperire pazienti, inoltre la parte etica è più delicata. Ben venga, quindi, l'aumento registrato perché servono più evidenze scientifiche".
pubblicità
Dal Rapporto Aifa emergono altri dati che confermano trend già in corso: circa la metà delle sperimentazioni condotte nel 2018 è in ambito oncologico ed emato-oncologico. Inoltre continua il trend in rialzo dei trial in malattie rare, che rappresentano il 31,5% del totale (erano il 25,5% nel 2017). Crescono, infine, le sperimentazioni no profit, sono state 182 nel 2018 e rappresentano il 27% del totale, 9 di queste promosse dalla Fondazione Irccs Istituto Nazionale Dei Tumori. Il generale dato positivo riscontrato, scrive Aifa, "potrebbe riflettere una prima ricaduta dell'avvicinarsi della Brexit, con lo spostamento degli sponsor verso altri Stati membri" o "un aumento di fiducia a seguito della pubblicazione della Legge 3/2018" in materia di sperimentazioni cliniche, che prevede tra l'altro la semplificazione di alcuni adempimenti formali.
I Correlati
Asco, melanoma: frontiere aperte alla “superimmunoterapia”. Con un tris di farmaci la sopravvivenza arriva al 72% nei casi gravi
Ascierto: "La combinazione di nivolumab, relatlimab e ipilimumab aumenta del 20% il tasso di sopravvivenza alla malattia rispetto alla somministrazione di due immunoterapici insieme"
Funziona nei topi un farmaco antietà con meno effetti collaterali
Contrasta diabete e arteriosclerosi e prolunga la durata della vita
Ritornano i farmaci psichedelici per le cure mentali
Gli esperti: "Cautela, ma enorme potenziale terapeutico"
Dal dolore alla speranza: La Palmitoiletanolamide come rimedio per le fasi della vita femminile: Endometriosi, Gravidanza e Menopausa
Ogni fase porta con sé un insieme unico di esperienze e cambiamenti fisiologici. Tuttavia, una costante accomuna molte di queste fasi: la suscettibilità della donna allo stato infiammatorio e al dolore
Ti potrebbero interessare
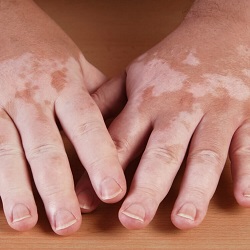
Vitiligine, sì dell'AIFA alla rimborsabilità della prima crema efficace
Il farmaco consente la repigmentazione della pelle dei pazienti sia sul viso che sul corpo
Oltre un nuovo farmaco su tre autorizzato per curare i tumori
Secondo i dati del Rapporto Horizon Scanning di Aifa, sono stati autorizzati 89 nuovi medicinali, di cui 48 contenenti nuove sostanze attive, 8 biosimilari, 23 equivalenti e 10 tra medicinali ibridi
Incontro Aifa-Egualia, Nisticò: Al lavoro per assicurare che tutti i farmaci essenziali siano disponibili per i pazienti italiani
“La lotta al fenomeno delle carenze passa anche attraverso il riconoscimento delle necessità di rendere economicamente sostenibili molti farmaci essenziali. Siamo al lavoro su questo aspetto”
Aifa, la carenza di ACE-inibitori in soluzione iniettabile in crisi renale sclerodermica (SRC) non dà rischi per i pazienti
I medicinali a base di enalapril iniettabile non sono disponibili in Italia da oltre vent’anni, in seguito alla revoca dell’Autorizzazione all’Immissione in Commercio (AIC) su rinuncia da parte dell’azienda farmaceutica titolare, nel 2000
Ultime News
Obesità, a luglio il pdl. L’Italia può diventare il primo paese al mondo con una legge su questa malattia
La proposta di legge di iniziativa dell’On. Roberto Pella è stata approvata il 28 maggio in Commissione Affari Sociali della Camera, ed è stata calendarizzata per la votazione in Aula
Enpam, medici di famiglia: così saranno le case di comunità Spoke. Oliveti, il rilancio della professione passa dall’aggregazione
Il fondo immobiliare che realizzerà le case "spoke" le affiderà ai medici interessati in affitto o in leasing
Al via Sognando Itaca, progetto mirato alla riabilitazione psico-sociale dei pazienti ematologici
L’impegno di AIL per Ambiente e Salute. Parte da Genova il viaggio solidale in 8 tappe lungo il Mar Tirreno
Asco, melanoma: frontiere aperte alla “superimmunoterapia”. Con un tris di farmaci la sopravvivenza arriva al 72% nei casi gravi
Ascierto: "La combinazione di nivolumab, relatlimab e ipilimumab aumenta del 20% il tasso di sopravvivenza alla malattia rispetto alla somministrazione di due immunoterapici insieme"








Commenti